



WDR5是一个高度保守的蛋白质,与20多个蛋白质直接相互作用,包括组蛋白H3K4甲基转移酶MLL/SET1复合体和纺锤体组装蛋白KIF2A,在细胞核和细胞质中都有重要生物学功能1。然而WDR5在众多复合体间如何有序转换而不造成紊乱研究不明。此外,WDR5在多种癌症中高表达,是一个潜在的癌症靶标。当前已有多个靶向WDR5 WIN位点的抑制剂被开发成潜在抗癌药物,其基础是抑制WDR5与MLL/SET1复合体的结合,进而调控H3K4甲基化修饰以抑制癌细胞增殖2。然而近期的研究表明多个药物虽然能抑制癌细胞增殖,但不影响H3K4甲基化修饰3,4,暗示这些药物的作用机制研究不明,可能抑制了WDR5与其他蛋白质的结合进而影响癌细胞的增殖。因此,阐明WDR5如何在众多互作蛋白间被时空调控不仅有重要的科研价值,也对安全有效地开发靶向WDR5的药物有指导意义。
最近的研究发现人基因组除了编码已知的2万多个蛋白质,还可能编码几千个小蛋白质(小于150个氨基酸),目前已有20多个被证实存在且有重要生物学功能,发现和功能研究这些未注释(Unannotated)小蛋白质已成为一个新兴研究热点5,6。2023年9月26日,华东师范大学曹雄文课题组(课题组博士后陈嫣然为第一作者)与耶鲁大学Sarah A. Slavoff课题组合作在Cell Reports上发表了研究论文Unannotated microprotein EMBOW regulates the interactome and chromatin and mitotic functions of WDR5。课题组发现人SCRIB基因的5'UTR编码一个未注释小蛋白质EMBOW,EMBOW结合并调控WDR5与其他蛋白质的相互作用,进而调控WDR5相关的染色质和纺锤体组装功能。这些结果显示EMBOW是一个重要的WDR5调控因子。

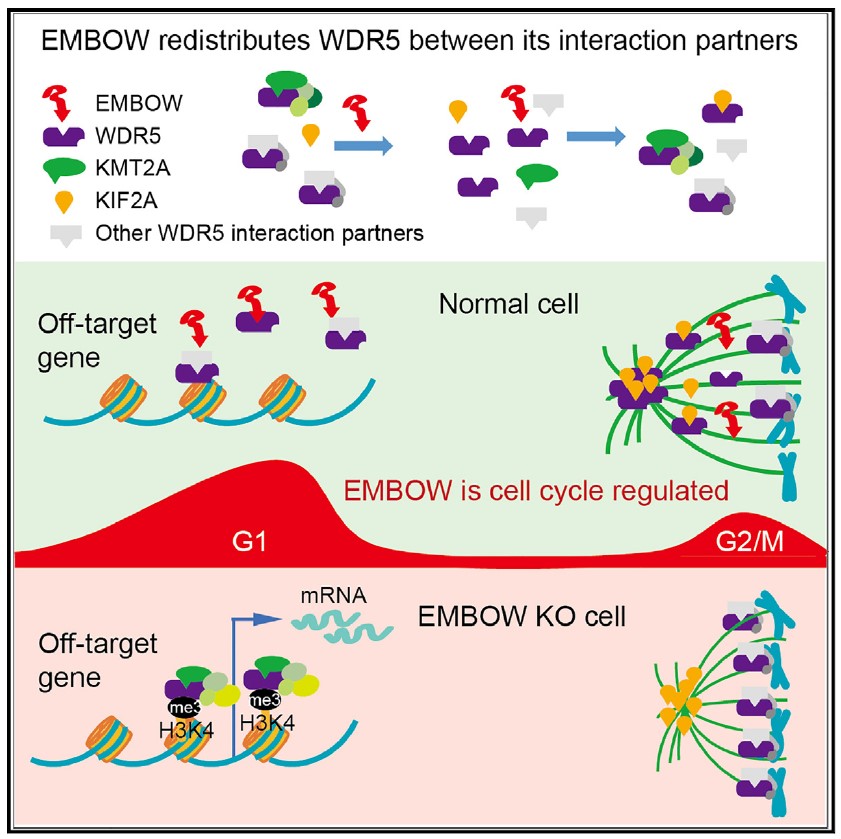
为了功能研究实验室前期找到的未注释小蛋白质EMBOW,研究人员首先利用免疫沉淀偶联质谱(IP-MS)实验鉴定了EMBOW的相互作用蛋白质,发现其主要结合WDR5。进一步的结合结构域定位发现EMBOW蛋白质的第二位精氨酸与WDR5的WIN位点结合。随后研究人员利用非标记定量质谱发现EMBOW调控WDR5与其他WIN位点结合蛋白的互作,包括KMT2A/MLL1和KIF2A。进一步的功能研究发现缺失EMBOW导致WDR5在细胞分裂中期纺锤体上的定位异常,降低WDR5与KIF2A的结合,进而导致纺锤体缩短,细胞生长变慢;另一方面,缺失EMBOW促进WDR5与KMT2A的结合,导致KMT2A复合体错误地定位于off-target基因的promoter区域,进而促进这些基因的H3K4me3修饰水平和转录。有意义的是,研究人员发现EMBOW本身严格受细胞周期调控,在G1后期和G2/M期有两个表达高峰。综合这些数据,研究人员得出结论:EMBOW在细胞周期中时空调控WDR5在不同复合体间的转运,保证WDR5在染色质和纺锤体上正常工作,说明EMBOW是一个重要的WDR5调控因子。
耶鲁大学化学系Slavoff教授和华东师范大学生命科学学院曹雄文研究员为本文的共同通讯作者,曹雄文课题组的博士后陈嫣然和Slavoff课题组的博士后苏浩淼为本文的共同第一作者。该研究得到了复旦大学基础医学院汪振天课题组和华东师范大学生命科学学院翁杰敏课题组的大力支持,受到上海市浦江人才计划和国家自然科学基金等项目的资助。
曹雄文课题组致力于寻找、鉴定和功能研究未注释小蛋白质。着重开展两方面的研究:1)以基因表达丰富的小鼠睾丸为模型,寻找和鉴定与雄性生殖相关的未注释小蛋白质,并进行功能研究;2)与复旦大学基础医学院汪振天课题组合作,以胰腺癌为模型,寻找和鉴定与胰腺癌发生发展相关的未注释小蛋白质,并进行功能研究。课题组成立于2023年1月,欢迎有兴趣的研究生和博士后加入团队。
原文链接
https://www.sciencedirect.com/science/article/pii/S2211124723011579
参考文献
1. Guarnaccia, A.D., and Tansey, W.P. (2018). Moonlighting with WDR5: A Cellular Multitasker. Journal of clinical medicine 7. 10.3390/jcm7020021.
2. Chen, X., Xu, J., Wang, X., Long, G., You, Q., and Guo, X. (2021). Targeting WD Repeat-Containing Protein 5 (WDR5): A Medicinal Chemistry Perspective. Journal of medicinal chemistry 64, 10537-10556. 10.1021/acs.jmedchem.1c00037.
3. Siladi, A.J., Wang, J., Florian, A.C., Thomas, L.R., Creighton, J.H., Matlock, B.K., Flaherty, D.K., Lorey, S.L., Howard, G.C., Fesik, S.W., et al. (2022). WIN site inhibition disrupts a subset of WDR5 function. Scientific reports 12, 1848. 10.1038/s41598-022-05947-9.
4. Aho, E.R., Wang, J., Gogliotti, R.D., Howard, G.C., Phan, J., Acharya, P., Macdonald, J.D., Cheng, K., Lorey, S.L., Lu, B., et al. (2019). Displacement of WDR5 from Chromatin by a WIN Site Inhibitor with Picomolar Affinity. Cell reports 26, 2916-2928 e2913. 10.1016/j.celrep.2019.02.047.
5. Chen, J., Brunner, A.D., Cogan, J.Z., Nunez, J.K., Fields, A.P., Adamson, B., Itzhak, D.N., Li, J.Y., Mann, M., Leonetti, M.D., and Weissman, J.S. (2020). Pervasive functional translation of noncanonical human open reading frames. Science 367, 1140-1146. 10.1126/science.aay0262.
6. Prensner, J.R., Enache, O.M., Luria, V., Krug, K., Clauser, K.R., Dempster, J.M., Karger, A., Wang, L., Stumbraite, K., Wang, V.M., et al. (2021). Noncanonical open reading frames encode functional proteins essential for cancer cell survival. Nature biotechnology 39, 697-704. 10.1038/s41587-020-00806-2.