现代药剂学不仅需要高分子药物载体能够在一定的刺激下触发药物释放,而且要在外界环境改变之后适时停止药物释放,从而实现按需递药(on-demand delivery)。按需递药可以最大程度上提高药物的利用度,延长药效持续时间,并降低药物暴释等风险。最近的一项研究中,华东师范大学的程义云和张强等研究人员发明了一种新型响应性水凝胶。该水凝胶可以实施近红外光可控的“开关式”药物释放。相关研究发表在2017年2月份的Chemistry of Materials杂志上(A Polydopamine Nanoparticle-Knotted Poly(ethylene glycol) Hydrogel for On-Demand Drug Delivery and Chemo-photothermal Therapy, Chem. Mater. 2017, 29, 1370-1376。2016年影响因子: 9.407)。
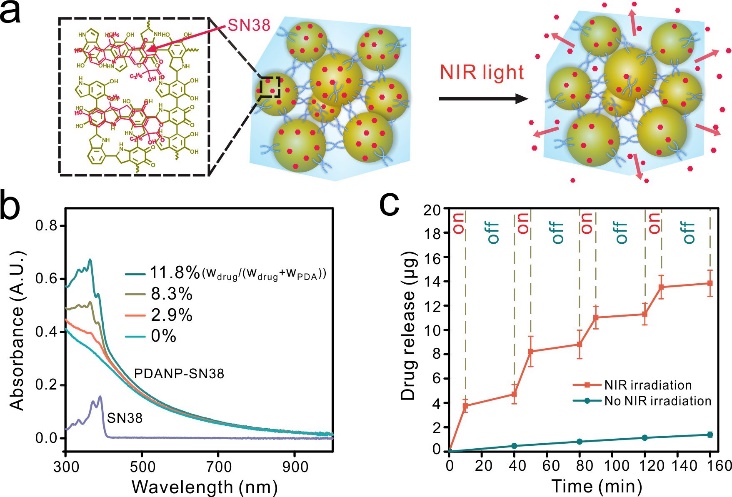
图1. 聚多巴胺和多臂聚乙二醇交联形成的水凝胶能够有效负载抗肿瘤药物SN38,
并在近红外光的照射下触发其释放。
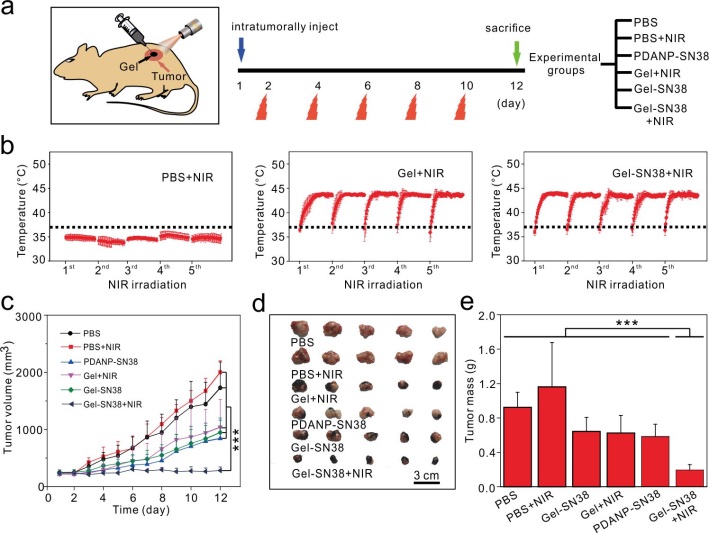
在该研究中,研究人员利用具有类黑色素性质的聚多巴胺纳米颗粒作为交联剂与多臂聚乙二醇(巯基末端)反应形成水凝胶网络。聚多巴胺纳米颗粒作为水凝胶网络的关键组成部分同时担负两项重要功能:一是利用其表面和药物分子之间的π-π stacking装载药物(如SN38),二是利用聚多巴胺纳米颗粒的光热转换性能。研究人员发现装载在该水凝胶中的化疗药物在生理条件下具有很好的稳定性,而当水凝胶置于近红外光照射的条件下,药物可以实现“开关式”响应释放(图1)。该功能的独特之处在于不仅可以通过红外光来触发药物释放,而且可随时撤去红外光来关闭药物释放的通道,从而实现按需递药。由于水凝胶可以将聚多巴胺纳米颗粒长期封锁在肿瘤病灶或其周边组织,因此具有一次给药多次治疗的功效,从而进一步提高了癌症治疗的效果。动物实验结果很好地证实了该水凝胶在体内同样可以实现红外光介导的药物按需递送,有效地抑制了肿瘤的生长(图2)。在长达四个月的体内植入实验中,研究人员没有发现相关的异物反应现象,也没有检测到任何血液或组织毒性。
图2. 光控SN38释放有效抑制了肿瘤的生长。该水凝胶可实现一次给药,多次治疗。