



让细胞“听懂”人为指令,在特定的时间、空间精准调控治疗蛋白药物的表达和释放,不再是科幻小说中才有的情节,而是医学合成生物学的前沿领域。合成生物学使我们能够按照用户自定义的需求,对细胞进行有目的的设计、改造和重编程。装载有人工基因线路的定制细胞,就像一个智能“细胞药物工厂”,通常情况下处于休眠状态。当感受到外界指令如小分子药物,病理标志物或光、电等物理信号后,它们则会迅速苏醒,对外界信号进行处理和计算,随后按需生产释放蛋白药物。
现有的人工定制细胞虽然在疾病治疗领域取得了一定的进展,然而它们对外界指令的响应、分析及处理速度仍然处于“1.0版本”的缓慢响应阶段。主要原因为这类定制细胞大部分都基于对治疗蛋白药物转录或翻译水平的调控,当细胞感受到外界指令后,需要数小时甚至数天才能表达释放出足量的蛋白药物,无法满足对有即时用药需求的疾病治疗,如哮喘、心绞痛、疼痛等。
为解决上述人工定制细胞‘开机’缓慢的问题,华东师范大学生命科学学院、上海市调控生物学重点实验室、医学合成生物学研究中心叶海峰研究团队通过重编程蛋白质分泌途径,开发了一个精准可控的蛋白质快速释放技术平台PASS系统,实现了蛋白药物分钟级别的可控释放。这一创新成果“A programmable protease-based protein secretion platform for therapeutic applications”于2023年10月23日发表在国际期刊Nature Chemical Biology。
快速了解精准可控的蛋白质快速释放技术平台PASS系统
叶海峰研究团队介绍,PASS最初的设计基于这样一个设想:省略现有定制细胞对蛋白药物缓慢的转录、翻译以及加工等步骤,将足量的蛋白药物提前生产好,储存在细胞的某个“仓库”中,只要控制仓库门的打开,就可以实现对蛋白药物的可控快速释放。
研究人员基于细胞内蛋白质的分选原理,成功实现了这一目的。具体而言,他们通过一段内质网回收信号将提前翻译好的目的蛋白锚定在细胞“内质网仓库”中,以备用时之需。他们在内质网回收信号和目的蛋白之间融合了一段可以被蛋白酶识别的肽链,当这个“链子”被蛋白酶水解切除时,锚定在内质网上的治疗蛋白就会迅速释放到细胞外。随后,研究人员通过调控蛋白水解酶的活性,设计构建了三种精准可控的蛋白质快速释放系统,分别为小分子调控的蛋白质快速释放系统chemPASS,响应肿瘤抗原的杀伤蛋白快速释放系统antigenPASS以及光诱导调控的蛋白质快速释放系统optoPASS (图1)。
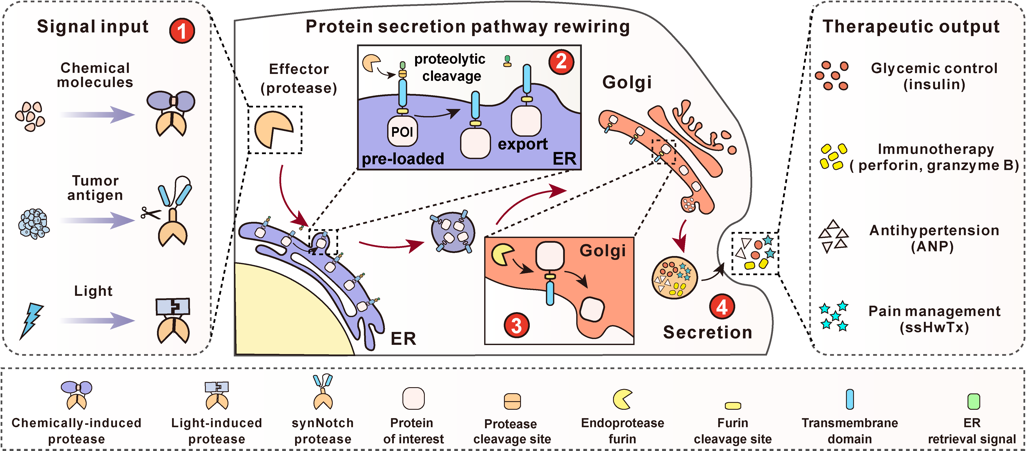
图1.PASS的设计原理图
研究人员将装载有chemPASS基因线路的定制细胞移植到1型糖尿病小鼠体内,当小鼠口服小分子药物后,仅需30分钟就可有效诱导胰岛素的释放,实现快速降血糖(图2)。
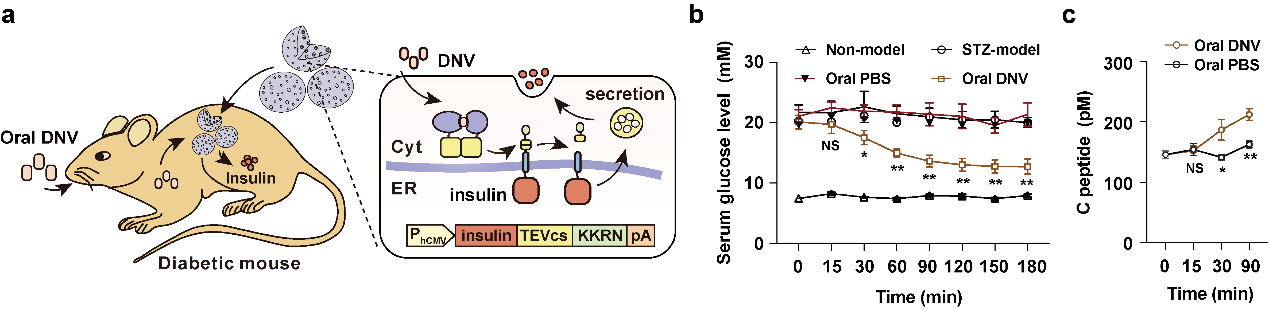
图2.ChemPASS定制细胞对1型糖尿病小鼠血糖的调控
装载有antigenPASS的免疫T细胞可精准识别肿瘤细胞,释放杀伤蛋白穿孔素(Perforin)或颗粒酶B(Granzyme B),从而有效杀死肿瘤细胞(图3)。
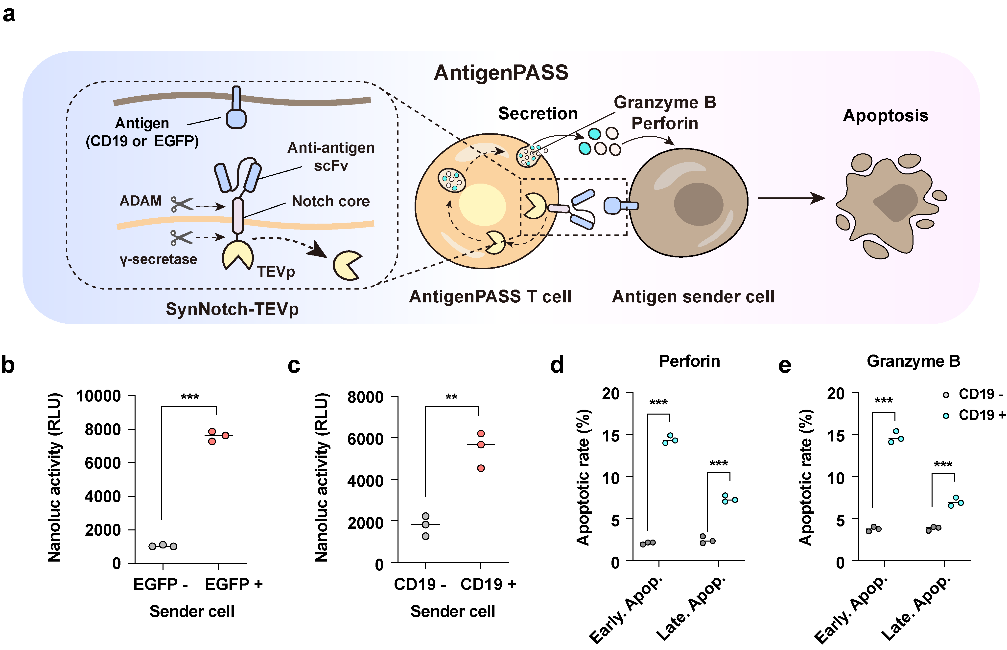
图3.AntigenPASST细胞诱导靶细胞凋亡
只需要一束光,就可以诱导装载有optoPASS基因线路的人工定制细胞快速释放降压肽、降糖肽、止疼肽。实验证明,将optoPASS定制化细胞植入1型糖尿病、高血压以及慢性炎症性疼痛小鼠模型的皮下,仅需光照15分钟,就能诱导治疗肽的释放,实现快速降血糖、降血压以及镇痛的效果(图4)。
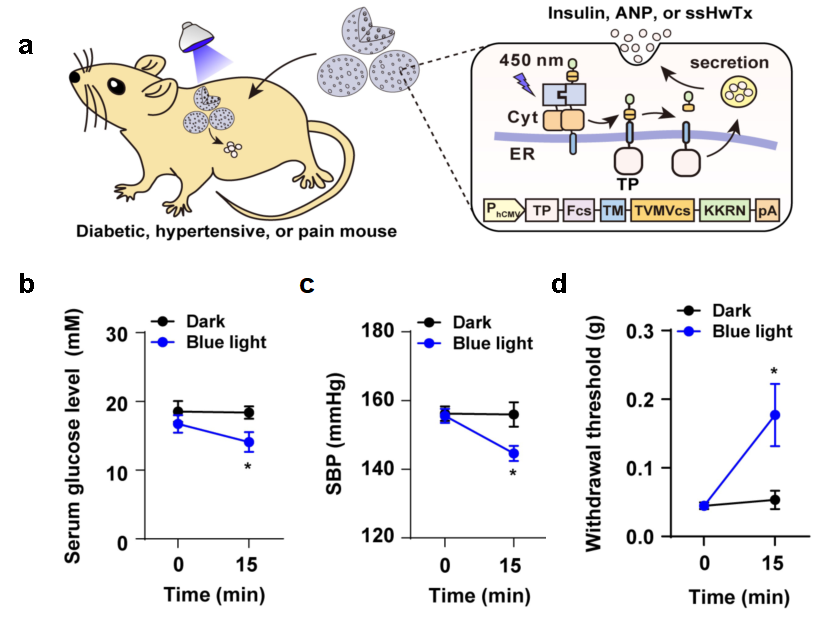
图4.OptoPASS定制细胞在多种疾病模型小鼠中的应用
综上所述,研究人员开发了一个精准可控、快速响应外部信号指令且在分钟级别释放蛋白药物的蛋白质快速释放技术平台PASS,为基础生物学研究和精准可控的基因治疗和细胞治疗提供了切实可行的蛋白药物瞬时递送新方案。

该设计图主要描绘了细胞内的基因线路PASS控制系统,特别是基因线路控制系统与细胞内质网的相互作用。示意图的关键概念是锚定在内质网治疗蛋白受外界信号控制释放,如光照等信号。
2020级博士研究生王欣怡和2021级博士研究生康利萍为该论文的共同第一作者。

左起:2020级博士研究生王欣怡、叶海峰研究员、2021级博士研究生康利萍
附:
论文链接:https://www.nature.com/articles/s41589-023-01433-z
新闻来源:
华东师范大学官网(学术卓越栏目):https://www.ecnu.edu.cn/info/1094/64764.htm